2023年8月21日,杭州尚健生物技术有限公司(以下简称“尚健生物”)宣布,其自主研发的1类创新型治疗用生物制品注射用SG1827获得国家药品监督管理局(NMPA)批准开展临床试验,适应症为晚期恶性实体瘤。
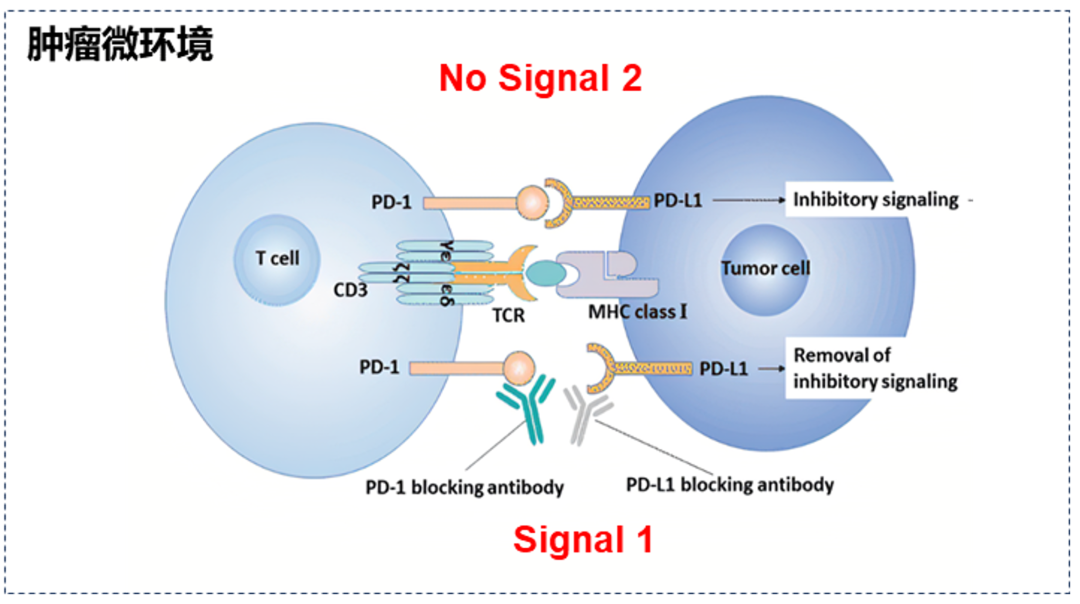
免疫应答过程中T细胞的激活需要双信号刺激,第一信号来自TCR识别MHC/抗原肽复合物,传递抗原特异性识别信号;第二信号由APC的共刺激分子提供,为非特异性协同刺激信号。作为肿瘤免疫治疗的代表,抗PD-1/PD-L1抗体通过阻断PD-1/PD-L1信号通路,解除该信号通路对免疫系统的抑制作用,可以一定程度上使T细胞活化从而起到杀伤肿瘤细胞的作用;但由于肿瘤微环境中缺少足够的T细胞共刺激信号,从而导致T细胞活化“受损”,是肿瘤免疫治疗的低反应率、原发或获得性耐药等问题的重要因素之一。多种策略协同激活T细胞,在增强其抗肿瘤活性的同时确保安全性,是近年来肿瘤免疫治疗的重要研究方向。
SG1827的主要作用机制之一是为T细胞活化提供共刺激信号,这对于促进免疫细胞对肿瘤的识别和攻击具有重要作用,有助于提高抗PD-1/PD-L1抗体治疗等免疫治疗的临床疗效。前期研究显示,SG1827单药以及联合其他免疫检查点抗体,均呈现出显著的抗肿瘤活性,且均未见明显的细胞因子释放反应,具有良好的安全性。
尚健生物创始人吕明博士表示:“SG1827作为尚健生物在‘后PD-1时代’最重要的产品管线布局之一,是公司第九个进入临床阶段的项目。SG1827药理学机制清晰、药效明确、安全性良好;前期研发过程中通过针对性分子设计,显著优化了PK特征,提高分子成药性,使SG1827在同靶点全球研发竞争中居领先地位的同时,具备成为Best in Class药物的潜力。我们将积极推进SG1827临床研发,争取让更多的肿瘤患者尽早获益。”